Une initiative européenne pour améliorer la chirurgie du foie
Date:
Mis à jour le 03/01/2024
Bien qu'il ne soit pas le plus fréquent, le cancer du foie est l'un des plus meurtriers, avec environ 900 000 décès dans le monde en 2020. Différentes options thérapeutiques peuvent augmenter les chances de survie, l'une d'entre elles étant l'ablation chirurgicale de la tumeur. Mais couper à travers un organe mou et s'assurer que la tumeur est entièrement réséquée tout en épargnant autant de tissus sains que possible n'est pas un mince défi.
En réunissant la réalité augmentée, la segmentation et l'amélioration d'images, le calcul haute performance, la modélisation biomécanique physiquement précise et bien d'autres domaines scientifiques, le projet européen Hipernav a voulu s'attaquer à plusieurs des goulets d'étranglement de la navigation chirurgicale. Il a été coordonné par Ole Jakob Elle, responsable du groupe de cybernétique médicale et de traitement des images à l'hôpital universitaire d'Oslo. Cet hôpital central de Norvège prend en charge toutes les transplantations et les traitements de cardiopathies congénitales du pays, ainsi qu'une grande partie de sa recherche biomédicale.
À ce jour, la plupart des résections de tumeurs hépatiques sont réalisées par chirurgie ouverte, et même ainsi, les tumeurs peuvent être difficiles à localiser, à atteindre ou à enlever. Les chirurgiens s'appuient sur différentes images préopératoires pour identifier les régions de l'organe qui doivent être enlevées et celles qui ne doivent pas être compromises, en particulier les veines et les artères du foie. Habituellement, les cliniciens utilisent une combinaison de techniques d'imagerie (imagerie par résonance magnétique, ultrasons, scanner...) pour obtenir l'image la plus précise possible du foie du patient. Ces images permettent aux chirurgiens de visualiser une vue de l'organe, coupe par coupe.
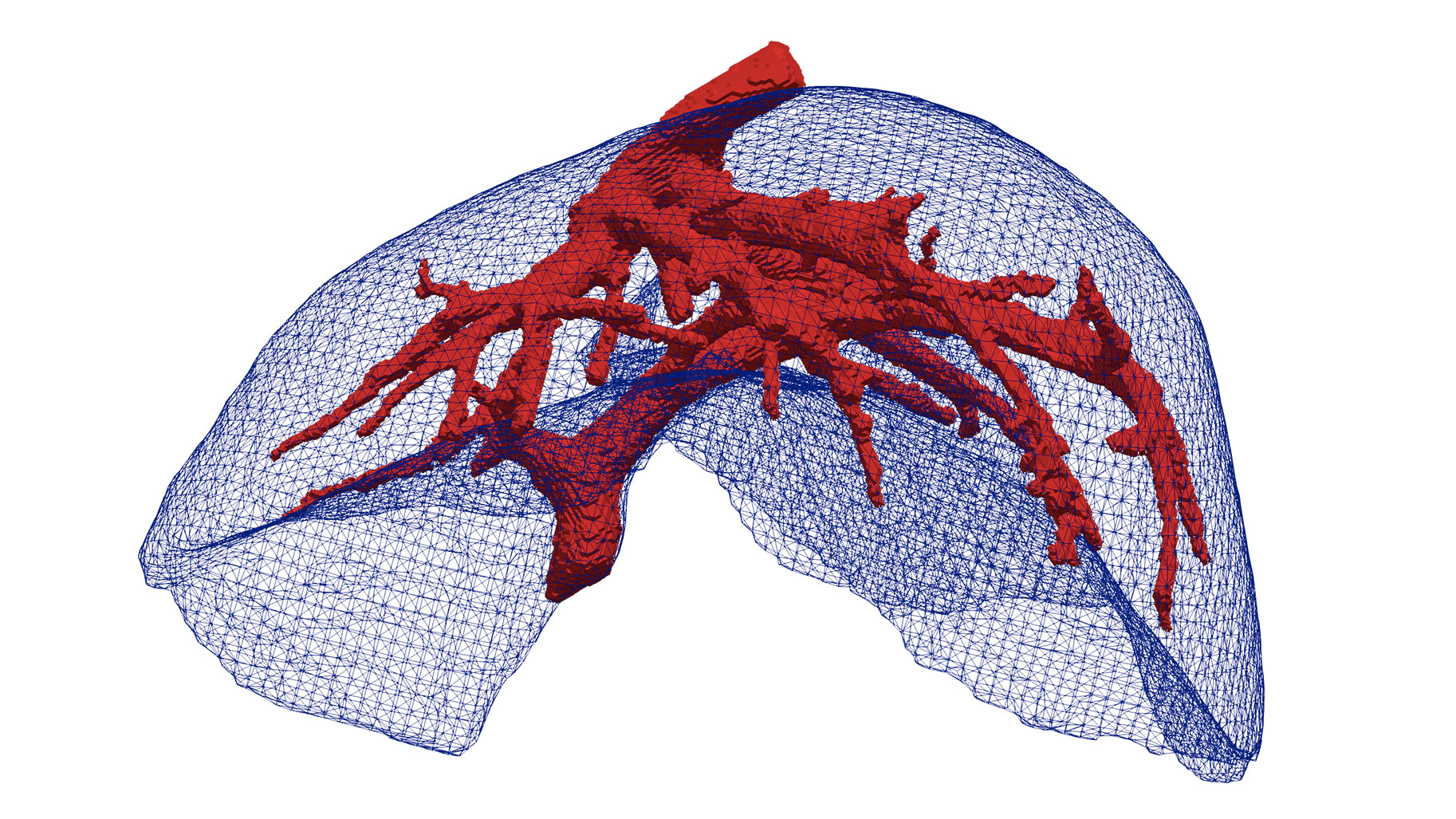
Pour aider à identifier les différentes structures (anatomiques) de l'organe, telles que la ou les tumeurs et les vaisseaux, ces images sont transformées en un modèle 3D. Cela aide le chirurgien à planifier le déroulement de la résection. Mais le foie est un organe très déformable. « Contrairement au cerveau, par exemple, qui se déforme peu lorsqu'on le manipule et est contraint par la boîte crânienne, la forme du foie change radicalement lorsque le patient change de position, respire ou lorsque l’on manipule l'organe avec des instruments chirurgicaux », souligne Ole Jakob Elle. Des données peropératoires sont alors nécessaires pour prendre en compte cette déformation et s'assurer que les incisions sont correctement réalisées.
Plus récemment, la chirurgie laparoscopique (également appelée cœlioscopie), où le chirurgien peut accéder à l'intérieur de l'abdomen par de petites incisions plutôt que par des coupes plus larges, s'est avérée réduire le temps de récupération du patient et améliorer sa qualité de vie. Mais pour réaliser ce type d'opération, il faut insuffler du CO2 dans l'abdomen, afin d’augmenter la taille du champ opératoire. Cette insufflation a un impact sur la forme du foie, et le fait de ne pouvoir visualiser le champ opératoire qu'à travers le laparoscope rend la chirurgie complexe et exige des simulations encore plus précises pour s'assurer que l’intervention soit réalisée en toute sécurité.
Le projet Hipernav, qui signifie "High-Performance soft tissue Navigation", a été lancé pour explorer ce que les techniques de modélisation et d'imagerie 3D les plus avancées pourraient apporter aux chirurgies minimalement invasives. Dans le prolongement de travaux antérieurs sur les apports possibles de la réalité augmentée à la laparoscopie, réalisés par Ole Jakob Elle et le chirurgien Bjorn Edwin, les quatorze partenaires du projet de recherche européen (voir encadré pour plus de détails) ont cherché, au cours des quatre dernières années, à rendre possible la chirurgie du foie, même pour les cas complexes au pronostic défavorable.
L'objectif final est de permettre, un jour, au chirurgien d'avoir accès en temps réel à un modèle virtuel précis du foie. Ce modèle devra prendre en compte les données préopératoires et peropératoires du patient et se déformer en fonction des propriétés biomécaniques des tissus mous pour aider l'équipe à naviguer dans l'organe tout au long du déroulement de l'opération. À terme, on pourrait envisager d'utiliser des systèmes de suivi et de navigation qui aideraient les cliniciens à évoluer autour des parties de l'organe à conserver et des tumeurs à retirer, « un peu comme votre GPS vous aide à diriger votre voiture sur une carte », indique Ole Jakob Elle.
Cela pourrait avoir un impact significatif sur le taux de survie des patients. En effet, en facilitant la préparation et la réalisation de l'opération par les chirurgiens, ce type de système permettra une meilleure résection et des opérations plus courtes. Et donc, une meilleure récupération pour le patient.
Pour atteindre l'objectif ambitieux du projet, de nombreux domaines disciplinaires doivent collaborer, de la bio-ingénierie au traitement des images en passant par les systèmes de navigation, le calcul à haute performance, les techniques de suivi, l'analyse et la planification des procédures chirurgicales … Tous ces domaines d'expertise clés ont été réunis par un plan coordonné de projets de recherche individuels s'attaquant à des défis spécifiques. Avec l'objectif de « former des chercheurs en début de carrière pour qu'ils acquièrent des compétences hautement transférables et deviennent des leaders internationaux dans leur domaine », ce réseau de formation innovant (ITN) a été financé par le programme de recherche et d'innovation Horizon 2020 de l'Union européenne grâce à une subvention Marie Skłodowska-Curie.
Le budget de quatre millions d'euros a permis de financer seize doctorants travaillant sur le projet en collaboration avec neuf des quatorze partenaires du réseau, selon les besoins des work packages. L'équipe de recherche MIMESIS d'Inria, dirigée par Stéphane Cotin, qui concentre ses recherches sur la simulation biomécanique en temps réel pour la formation et l’assistance peropératoire, était l'un de ces partenaires d'accueil.
Basée à Strasbourg, l'équipe de Stéphane Cotin a développé plusieurs modèles numériques pour la formation clinique en chirurgie ophtalmologique, hépatique, endovasculaire et rénale. L'une de leurs principales réalisations est un modèle biomécanique du foie qui tient compte des propriétés biophysiques des tissus mous et de l’anatomie du patient pour refléter avec précision la déformation de l'organe lorsqu'il est soumis à des contraintes, telles que celles exercées par les instruments chirurgicaux.
L'utilisation de ce modèle dans un contexte clinique, en l'adaptant aux données préopératoires d'un patient et en le combinant avec des données peropératoires actualisées (par exemple à l'aide d'images échographiques), pourrait faire une différence importante dans la réduction des risques opératoires. En effet, le fait de disposer d'un jumeau numérique de l'organe réel permet d'envisager une utilisation sûre des systèmes de navigation dans les tissus mous. En s'appuyant sur des techniques d'imagerie moins coûteuses que l'IRM ou le scanner CT, cette technologie pourrait également réduire le coût des opérations.
Bien sûr, toutes les étapes menant à un dispositif de réalité augmentée qui permettrait au chirurgien de visualiser l'organe en temps réel n'ont pas été franchies au cours des quatre années du projet Hipernav. Mais des résultats significatifs ont été obtenus dans plusieurs domaines clés, qu'il s'agisse de l'amélioration du modèle biomécanique, d'une meilleure estimation de la durée de l'opération basée sur l'analyse du flux de travail ou d'une diminution drastique du temps de calcul nécessaire à la mise à jour du modèle. La plupart des points à améliorer ayant été identifiés, un prochain ITN permettra peut-être d'aller encore plus loin dans la réalisation de cette chirurgie du foie du futur…
Partenaires ayant accueilli des doctorants
Organisations partenaires